ASÍ SERÁ EL COSTOSO FUTURO DE NUESTRA SALUD
El utópico y controversial Mundo feliz libre de enfermedades de Aldous Huxley parece estar cada vez más cercano. El triunfo sobre algunos tipos de cáncer, la diabetes y ciertos padecimientos psiquiátricos puede ser posible gracias a la secuenciación del conjunto de genes humanos. Un gran paso que también ha dado lugar, como era de esperarse, a una guerra de intereses económicos.

CUANDO el 12 de febrero de 2001 Craig Venter, presidente de la empresa estadounidense Celera Genomics, presentó ante la prensa los resultados del borrador del genoma humano, ya había consultado el valor de las acciones de su compañía. Mientras lo celebraba, supo que habían subido un 15% en una sola sesión y que habían conseguido arrastrar consigo al alza al sector de la biotecnología. Tenía doble motivo para brindar.
Ese día, fueron dos los grupos que presentaron sus resultados. El de Venter y el del consorcio público de Estados Unidos, Proyecto del Genoma Humano, formado por unos 20 laboratorios y más de 200 científicos que habían trabajado durante los diez últimos años. Con una compañía fundada hacía sólo tres, Venter se jactaba de que conseguiría un mapa del genoma humano mejor y más fácil de usar que el promovido por fondos estatales, el cual obtuvo tras 25 meses de inversiones multimillonarias. Y será su grupo el que se llevará los beneficios económicos de la investigación.
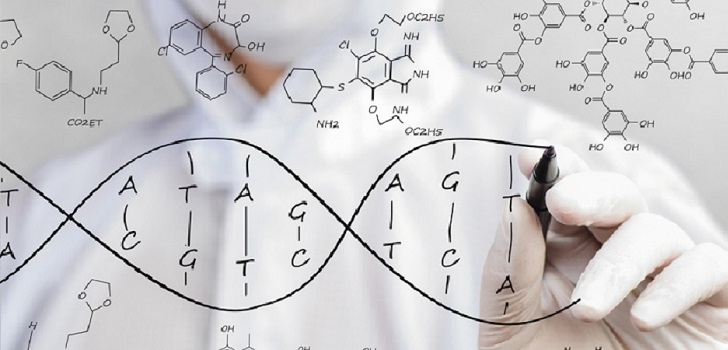
Libro de Instrucciones. El genoma es el conjunto de las instrucciones genéticas que sirven para ‘construir’ un ser humano y hacen que sea como es. En cada célula del cuerpo hay una copia igual de nuestro genoma –excepto óvulos y espermatozoides–. Está escrito en un alfabeto de cuatro letras –A, C, T y G–, y consta de tres mil millones de caracteres.
Con éstos, se forman palabras; es decir, los genes, que tienen instrucciones para fabricar las proteínas, sustancias fundamentales para que funcione el organismo. El conjunto de genes acabará configurando la novela de nuestra vida. Lo que presentaron los dos grupos de científicos fueron dos versiones de la misma obra, sólo que en este momento no tenemos claro el significado de muchas palabras y, además, hay zonas con espacios en blanco y sin puntos y comas, lo que dificulta la lectura. Por eso, la tarea de los científicos durante los próximos años será su desciframiento.
Los expertos en genética todavía no se ponen de acuerdo sobre cuál de las dos versiones presentadas es mejor: la secuenciación obtenida por Celera o la lograda por el grupo público. Pero la compañía estadounidense intenta que su mapa se convierta en un estándar en biotecnología, algo similar a lo que hizo Bill Gates con el software de Microsoft. Para su utilización han creado un sistema especial de pago: cada uno de sus 35 grandes clientes –laboratorios farmacéuticos y centros de investigación–, debe dar, al año, unos 13.8 millones de dólares. En cambio, los clientes medianos y pequeños sólo tendrán que aportar nueve millones, aunque deberán abonar después un porcentaje sobre los logros que consigan con su sistema. Y a los universitarios les cobrará unos 92 mil dólares. Por el momento, el navegador de Celera, que permite a los científicos acceder de forma fácil a los genes que buscan y entrar en su ‘libro de la vida’, está a punto de convertirse en un best seller.

La curación de enfermedades. Con la presentación del genoma humano se cierra una etapa y se abre otra nueva: la de la investigación que debe conducir a la curación de numerosas enfermedades genéticas –se calcula que hay alrededor de ocho mil patologías de origen genético, incluso la predisposición a constiparse lo es–. Los expertos aseguran que, dentro de unos años, conseguiremos diagnosticar todos los males de este tipo. Para ello, sólo hace falta señalar cuáles son los genes y las proteínas responsables de ellos.
Una de las grandes sorpresas de la cartografía del humano ha sido averiguar que el Homo sapiens únicamente posee unos 30 mil genes. El paso siguiente será descubrir qué función tiene cada uno. Las primeras pistas sobre la función de un gen se hallan en su secuencia y en la de su proteína. Y precisamente en esta última reside la auténtica clave de la lucha contra las enfermedades, porque los fármacos en realidad actúan sobre ellas. Los actuales sólo causan efecto sobre unas 500. Hasta llegar a las 30 mil, hay mucho trabajo y, por el camino, mucho dinero para el que lo consiga.
“Se compara el gen afectado con bases de datos de otros animales –como ratas–, y se busca suplir este gen. Lo utilizan las compañías farmacéuticas y se llama terapia génica”, explica María del Refugio Bermúdez-Cruz, profesora investigadora del Departamento de Genética y Biología del Centro de Investigación y Estudios Avanzados (CINVESTAV) del Instituto Politécnico Nacional (IPN).
Durante los diez años del Proyecto Genoma se identificaron 1,100 genes de unas 1,500 enfermedades. Mayoritariamente, son los de las principales patologías monogénicas, es decir, provocadas por un solo gen. Es el caso del síndrome de Down, el del cromosoma X frágil –que es la causa de retraso más frecuente–, o el de la fibrosis quística. Si en la familia de una persona se han dado casos de alguna de estas enfermedades, actualmente se pueden diagnosticar antes del embarazo y realizar una terapia preimplantacional. Y en parejas de riesgo se hace una fecundación in vitro, analizando antes los óvulos e implantando únicamente los que no tienen la enfermedad.
Unidos son más fuertes. Sin embargo, la propensión genética de las patologías más comunes no se debe a un solo gen, sino a varios, quizá a cientos que actúan simultáneamente. Desde el punto de vista genético, son complejas y, en cambio, son tan habituales como la hipertensión, el cáncer, el asma, la psoriasis, la diabetes o los trastornos psiquiátricos. Aún así, en algunas de ellas la investigación ha avanzado considerablemente y el conocimiento del genoma permitirá hacerlo todavía más.
Es el caso de algunos tipos de cáncer. Actualmente, si una mujer tiene antecedentes de cáncer de mama en su familia, puede conocer su predisposición a padecer la misma enfermedad. Para ello basta con realizarle una simple extracción de sangre y secuenciar en el laboratorio los genes BRCA1 y BRCA2 –situados en los cromosomas 17 y 13–. Además, si la mujer tiene una hermana, ésta no necesitará someterse al mismo análisis, ya que poseerá la misma mutación.
En México, según explica Bermúdez-Cruz, se pueden pedir secuencias de genes a Estados Unidos, “aunque ya contamos –el CINVESTAV y la UNAM–, con la tecnología para realizarlos en nuestro país, pero sólo en el área de investigación”, revela la experta.
Sin embargo, existen otros tipos de cáncer de los que todavía no se conoce nada, excepto que se trata de mutaciones genéticas de tipo maligno. Y aún no se sabe hasta qué punto influyen en ellas factores externos. En este sentido, “es necesario encontrar la correlación de algunos genes con la aparición de diversos tumores. El papiloma virus genital –que a largo plazo genera cáncer cervicouterino–, por ejemplo, es como la llave que enciende el automóvil, pero no es el motor, y debemos encontrarlo”, comenta Luis Marat, jefe del laboratorio de terapia génica del CINVESTAV.
Medicina a la carta. Lo cierto es que “los fármacos que ahora se emplean son muy restringidos, pues sólo atacan una de las causas y no funcionan en todos los pacientes. Las investigaciones del genoma permitirán entender cuáles son las proteínas y las vías metabólicas que se alteran y así diseñar fármacos o proteínas específicas que solucionen el problema de raíz”, declara María Teresa Tusié, investigadora titular del Departamento de Medicina del Instituto de Investigación Biomédica de la UNAM.
Precisamente hacia la búsqueda de nuevos medicamentos se dirige la acción de los laboratorios farmacéuticos, que se han lanzado a una loca carrera para hacerse de un negocio que será, sin duda, redondo. Los laboratorios que ya investigan sobre la información genética han empezado por patentar los genes. En Europa, la legislación no lo permite, pero en Estados Unidos sí –allí diversas compañías de biotecnología han registrado ya 700–. Aunque la política de patente del gen parece absurda cuando el consorcio público ha puesto a disposición de la humanidad el mapa del genoma, el negocio estará en las aplicaciones que se deriven de ello, en las bases de datos, en los procedimientos de análisis y, por supuesto, en encontrar los medicamentos adecuados.
Entonces podremos llegar a realizar una medicina a la carta. Un fármaco no actúa igual en dos pacientes con la misma enfermedad. El conocimiento del genoma permitirá afinar más a la hora de aplicar el más adecuado a cada persona.
El problema es que esto elevará los costos de la medicina predictiva, al tener que realizar multitud de pruebas genéticas. Para hacerse una idea, la secuenciación de un gen cuesta hoy en día cerca de 1,600 dólares; sólo hay que echar un cálculo sobre lo que significaría analizar enfermedades en las que están implicados varios genes. En la actualidad, instituciones como el Centro Médico Siglo XXI realizan investigación especializada –en la Unidad de Investigación Genética–. Y cabe pensar que en el futuro deberá afrontar el de todas si, como se prevé, la medicina del genoma se va abriendo paso como una nueva forma de entender la sanidad.
Pero lo cierto es que mucho deben cambiar sus presupuestos para que asuma unos costos tan elevados, sobre todo teniendo en cuenta que ahora cualquier prueba analítica ya tiene restricciones en función de los balances de cada departamento. Aún así, lo cierto es que, en teoría, una medicina predictiva bien aplicada debería disminuir los gastos, ya que si se puede diagnosticar que se desarrollará un tumor y se evita que lo haga, se producirá un ahorro personal y económico importante. Dentro de poco, las empresas y gobiernos deberán decidir cuáles de estas pruebas incluyen entre sus prestaciones gratuitas. En caso contrario, los usuarios tendremos que pagarlas de nuestro bolsillo.
Por otra parte, los laboratorios también disminuirán los gastos de salud y económicos que les supone aplicar una terapia incorrecta, ya que se eliminarán los costos provocados por los efectos adversos de los medicamentos, que no son pocos. En concreto, la administración estadounidense ha calculado que las reacciones desfavorables a los fármacos causan en ese país dos millones de hospitalizaciones anuales y que 100 mil de esos pacientes mueren. Los laboratorios tienen contabilizados estos gastos, y aunque normalmente no los hacen públicos, algunos practican una política más transparente, pues algunos llegan a pagar caro (hasta 4,760 dólares) por los efectos negativos –colitis ulcerosa digestiva–, que provocan los inmunodepresores que emplean. De ahí que muchos de éstos solucionen el problema con un simple análisis de sangre para realizar el fenotipo de los pacientes que lo consumen.
De lo que no hay duda es que la investigación genética aún depara muchas sorpresas, incluidos los conflictos, y quién sabe, tal vez el polémico Mundo feliz de Aldous Huxley no esté tan lejano.
* Tomado de revista mensual QUO.
Año 4, No, 44; Junio de 2001.
Ventaneando, Viernes 24 de Septiembre de 2021.